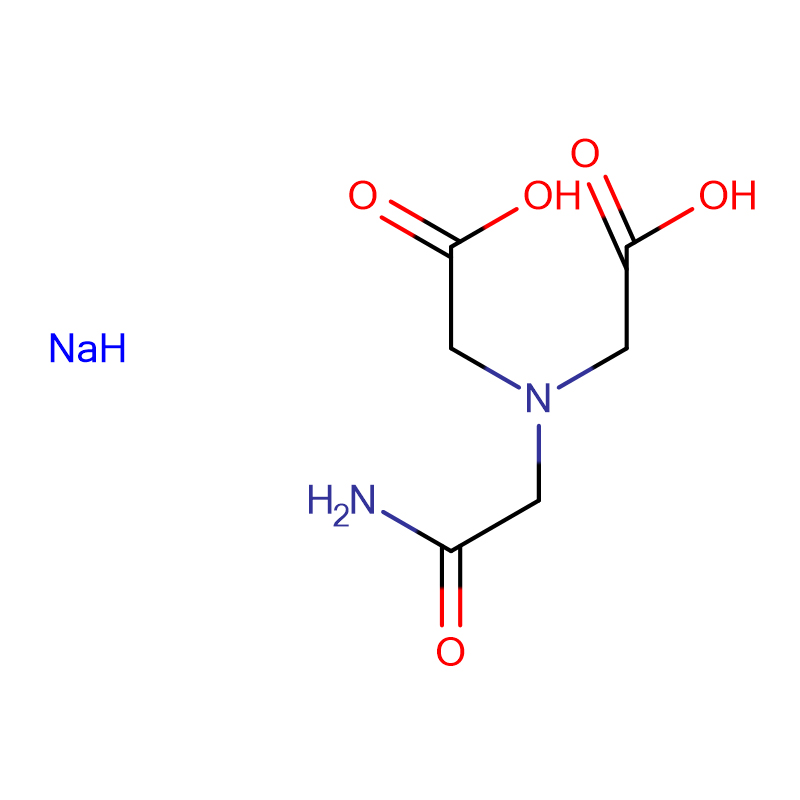
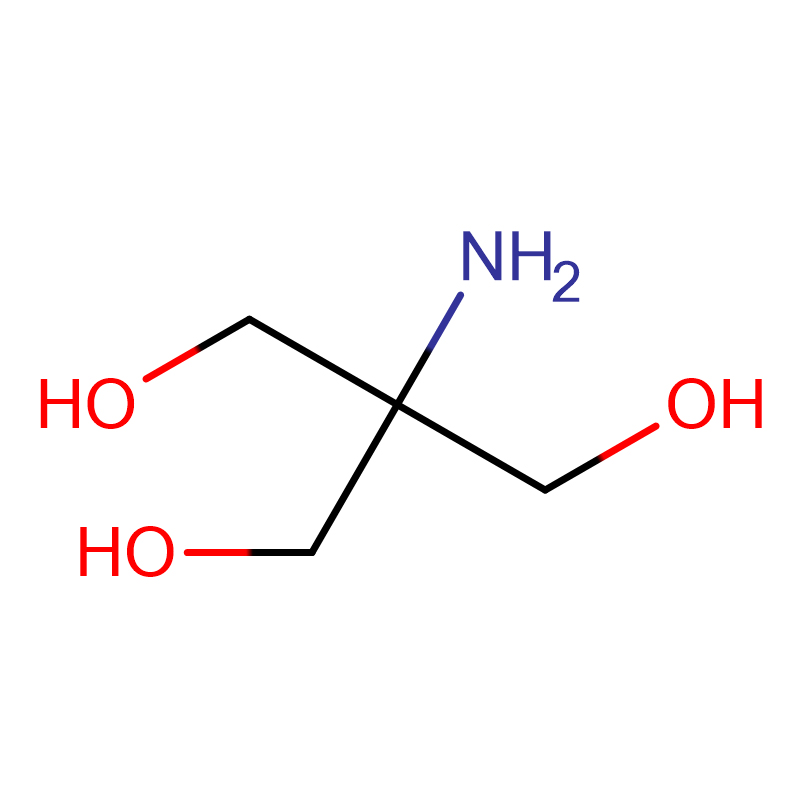
ADA DINODIUM SALT Cas:41689-31-0 N- (2- Amino- 2- oksoetyl)- N- (karboksymetyl) glycinedatriumsalt Hvitt krystallinsk pulver 98 %
| Katalognummer | XD90092 |
| Produktnavn | ADA DINODIUM SALT |
| CAS | 41689-31-0 |
| Molekylær formel | H2NCOCH2N(CH2CO2Na)2 |
| Molekylær vekt | 234,12 |
| Oppbevaringsdetaljer | Omgivende |
| Harmonisert tariffkode | 292419009 |
Produkt spesifikasjon
| Utseende | Hvitt krystallinsk pulver |
| Assay | >98,0 % |
| Lagringstemp | Butikk på RT |
Buffer er en løsning som kan motstå pH-endringer når en liten mengde syre eller alkali og vann tilsettes.pH-buffersystemet spiller en viktig rolle for å opprettholde den normale pH-verdien til organismer og det normale fysiologiske miljøet.De fleste celler kan bare operere i et veldig smalt pH-område.Det må ha et buffersystem for å motstå pH-endringene som oppstår under metabolismen.Det er tre hoved-pH-buffersystemer i organismen, de er protein- og bikarbonatbuffersystemer.Mengden av hvert buffersystem Det er forskjellig i ulike typer celler og organer.
Buffereffekten av bufferløsningen som består av den svake syren HA og dens salt NaA på syren skyldes tilstedeværelsen av en tilstrekkelig mengde alkali A- i løsningen.Når en viss mengde sterk syre tilsettes denne løsningen, blir H-ioner i hovedsak konsumert av A-ioner:
Derfor er pH-verdien til løsningen nesten uendret;når en viss mengde sterk base tilsettes, forbruker den svake syren HA i løsningen OH-ioner og hindrer endringen av pH.
Tilsett en liten mengde sterk syre eller sterk base til bufferløsningen, pH-verdien til løsningen vil ikke endre seg mye, men dersom mengden syre eller alkali tilsettes vil bufferløsningen miste sin buffereffekt.Dette viser at bufferkapasiteten har en viss grense.
Bufferkapasiteten til en bufferløsning er relatert til konsentrasjonen av komponentene som utgjør bufferløsningen.Bufferløsningen sammensatt av 0,1 mol·L-1HAc og 0,1mol·L-1NaAc har større bufferkapasitet enn bufferløsningen på 0,01mol·L-1HAc og 0,01mol·L-1NaAc.Dette kan bekreftes ved beregning.Konsentrasjonen av komponentene i bufferløsningen bør imidlertid ikke være for stor, ellers kan ikke interaksjonen mellom ionene ignoreres.